Главное
Израильская «Бонус Байогруп» (Bonus BioGroup) стала первой фармацевтической компанией в мире, разработавшей лекарственный препарат, который с невероятно высокой эффективностью помогает при протекающей в тяжелой форме коронавирусной инфекции COVID-19, вызванной коронавирусом SARS-CoV-2.
Оценочная эффективность «Мезенкьюэ» (MesenCure), который существенно снижает риск смерти и значительно сокращает время пребывания в больнице, превосходит таковую у всех прочих лекарств против тяжелого ковида приблизительно в четыре раза.
Назначение «Мезенкьюэ» пациентам, госпитализированным с тяжелым ковидом, оказалось настолько успешным, что впору говорить о прорывном достижении фармацевтической отрасли, стоящей в авангарде борьбы с пандемией COVID-19.
В январе 2022 года «Бонус Байогруп» отправила израильскому регулятору клинические данные «Мезенкьюэ» в целях одобрения этого антиковидного лекарственного средства.
«Мезенкьюэ» органично дополнит постепенно растущий арсенал противовирусных препаратов для лечения и профилактики COVID-19, таких как «Веклури» (Veklury, ремдесивир), моноклональные антитела, «Паксловид» (Paxlovid, нирматрелвир + ритонавир), «Лагеврио» (Lagevrio, молнупиравир), «МИР 19» (MIR 19).

«Мезенкьюэ»: подробности клинической проверки
Клиническое исследование NCT04716998 фазы II (рандомизированное, открытое, плацебо-контролируемое, многоцентровое) охватило взрослых пациентов, госпитализированных с тяжелой коронавирусной инфекцией COVID-19, характеризующейся диффузной пневмонией, острым воспалением, кислородной сатурацией ≤ 93%, жизнеугрожающим нарушением дыхания.
Участникам назначали «Мезенкьюэ» (внутривенно до трех доз) поверх стандартной терапии ковида либо только последнюю.
Промежуточные результаты
Согласно промежуточному анализу данных, 30-дневная частота выживаемости составила 94,0% (n=47/50) в группе «Мезенкьюэ» — против 23,3% (n=14/60) в группе стандартной терапии. Таким образом, добавление «Мезенкьюэ» к стандартному лечению COVID-19 привело к снижению вероятности летального исхода на 75,2%.
Применение «Мезенкьюэ» почти вдвое сократило период пребывания в больничном учреждении: с усредненных 17,2 дня в группе стандартной терапии — до 9,4 дня в группе экспериментального лечения. При этом треть больных ковидом в тяжелой форме, получавших израильский препарат, были выписаны из больницы в день окончания лечения, тогда как две трети — в течение последующих двух дней.
Профиль безопасности «Мезенкьюэ» характеризовался приемлемой переносимостью и отсутствием серьезных побочных реакций.
Итоговые результаты
Согласно итоговому анализу данных, охватившему клинические исходы 50 пациентов в группе «Мезенкьюэ» и 150 больных в контрольной группе, результаты экспериментального лечения тяжелого ковида получились следующими.
Добавление «Мезенкьюэ» к стандартной терапии COVID-19 обеспечило относительное снижение уровня летальности на 68% и уменьшение необходимости в инвазивной вентиляции легких на 57%.
Подключение «Мезенкьюэ» привело к сокращению продолжительности пребывания в больнице: свыше 50% пациентов выписались в течение двух дней после лечения, почти четверть (25%) — в день окончания лечения, а две пятых (40%) — через день.
Назначение «Мезенкьюэ» не сопровождалось какими-либо неблагоприятными событиями по части безопасности лечения.
Лечение коронавируса. «Паксловид»: новое лекарство от коронавируса. Все подробности
Пероральный противовирусный препарат Pfizer на 89% снизил риск госпитализации или смерти от ковида.
«Мезенкьюэ»: механизм действия
Лекарственный препарат «Мезенкьюэ» (MesenCure) представляет собой аллогенные мезенхимальные стволовые клетки (MSC), полученные из жировой ткани здоровых доноров.
Клетки в составе «Мезенкьюэ», которые предварительно примированы в целях усиления их иммуномодулирующих и противовоспалительных свойств и которые нацелены на подавление воспаления, регенерацию поврежденной легочной ткани и сдерживание цитокинового шторма, способствуют процессу выздоровления респираторной системы и других внутренних органов, пострадавших в результате прогрессирования коронавирусной инфекции.
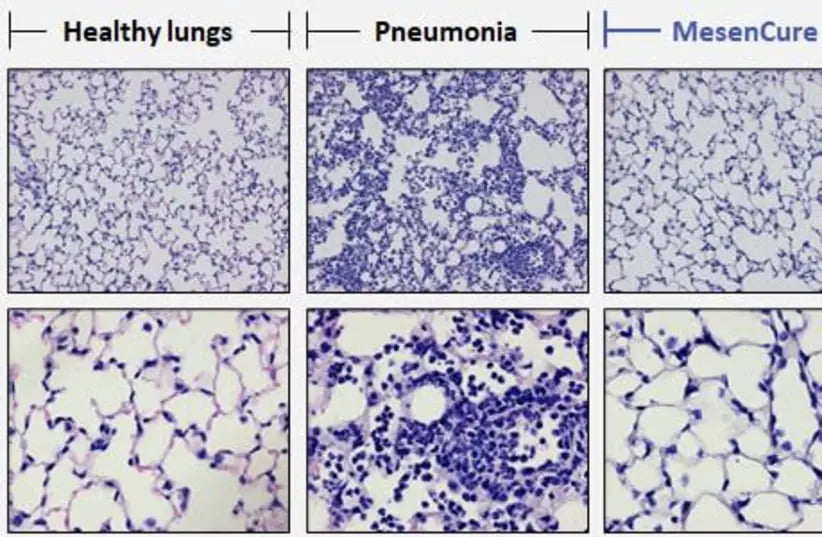
Иммуномодулирующие и противовоспалительные эффекты «Мезенкьюэ» реализуются благодаря модуляции пролиферации и активации иммунных клеток, опосредованной секрецией иммуносупрессивных факторов. После внутривенного введения клетки «Мезенкьюэ» накапливаются преимущественно в поврежденной легочной ткани. Секретируемые мезенхимальными клетками факторы роста кератиноцитов, эндотелия и гепатоцитов способствуют регенерации эпителиальных клеток легких, предотвращают апоптоз эндотелиальных клеток, восстанавливают альвеолярно-эпителиальный барьер, поврежденный цитокиновым штормом. Системно вводимые мезенхимальные клетки также спасают ковидных пациентов от острого повреждения миокарда и почек, аритмии, шока и смерти от полиорганной недостаточности.
Вообще «Мезенкьюэ» вполне пригоден для лечения острого респираторного дистресс-синдрома (ОРДС) и пневмонии, которые вызваны не только новым коронавирусом SARS-CoV-2, но и другими патогенами вирусной или бактериальной природы либо воздействием загрязняющих веществ.
Следует понимать, что «Бонус Байогруп» провела большую доклиническую работу над «Мезенкьюэ», дабы убедиться в терапевтической состоятельности. Так, в доковидную эпоху MSC привлекали большое внимание, но исследователям не удавалось продемонстрировать их эффективность в лечении ОРДС, высказывались также опасения на предмет гемосовместимости (зависит от исходной ткани, из которой получены MSC) и способа введения в организм (актуально при сопутствующих коагулопатиях). «Бонус Байогруп» довела до ума свой вариант MSC, полученных из жировых стромальных клеток (ASC) и затем примированных.
На животных моделях острого повреждения легких было продемонстрировано, что «Мезенкьюэ» на 60% уменьшает отек и на 40% снижает количество лимфоцитов в легочной жидкости. Три внутривенных дозы «Мезенкьюэ» спасли животных от смертельного исхода. In vitro препарат ингибировал пролиферацию активированных T-клеток на 83%. При охлаждении «Мезенкьюэ» сохранял свою иммуномодулирующую способность дольше, чем непримированные ASC, то есть был более стабильным продуктом, подходящим для длительного хранения. Гемосовместимость клеток «Мезенкьюэ» оказалась сходной с таковой для MSC из костного мозга, которые считаются безопасными для внутривенного введения. Об этом свидетельствовали на 50% сниженные уровни фактора свертывания крови 3 (F3) — его мРНК, белка и активности, а также более чем двукратное повышение уровня ингибитора пути тканевого фактора (TFPI), экспрессируемого на клетках «Мезенкьюэ».

Лечение коронавируса. Молнупиравир: новое эффективное лекарство от коронавируса. Все подробности
Молнупиравир поможет высокорисковым ковидным больным не загреметь в больницу или не умереть.
Согласно клиническим исследованиям на людях, эффективность «Мезенкьюэ» в лечении коронавирусной инфекции COVID-19 может быть связана с клеточной экспрессией de novo гена, кодирующего рецептор интерлейкина 6 (IL6R), что делает эти клетки более чувствительными к воспалению в сравнении с непрофессионализированными наивными мезенхимальными стромальными клетками (NA-MSC), а также с более чем 8-кратным повышением регуляции гена EDIL3, кодирующего эндогенный ингибитор иммунной инфильтрации.
Соответствующий иммуносупрессивный эффект «Мезенкьюэ», продемонстрированный in vitro, засвидетельствовал подавление активации T-клеток CD4 и CD8 двое эффективнее, чем это делают NA-MSC. Кроме того, «Мезенкьюэ» очень быстро подавлял выработку ROS первичными нейтрофилами.
В дополнение к местным иммуносупрессивным эффектам, наблюдаемым у тяжелых пациентов с COVID-19, которым назначали «Мезенкьюэ», отмечался значительный рост нейтрофилов и лимфоцитов в крови, связанное с количеством введенных доз препарата и отражающееся усилением периферического иммунитета, необходимого для успешной виремии.

«Мезенкьюэ»: экспертные комментарии
Ошеломительные клинические успехи «Мезенкьюэ» имеют далеко идущие последствия для пациентов и систем здравоохранения.
Во-первых, значительное сокращение времени пребывания в стационаре снизит нагрузку на и без того перегретую систему здравоохранения, высвободит ресурсы для более качественного ухода за другими пациентами, уменьшит экономическое бремя. Применение «Мезенкьюэ» снизит стоимость больничного лечения тяжелого ковида приблизительно на 40%.
По оценкам самой «Бонус Байогруп», сокращение срока больничного пребывания в реальной практике использования «Мезенкьюэ» может оказаться еще большим, так как многих из участников клинического испытания следовало отправить домой после введения первой или второй из трех доз препарата, но они оставались в больнице дольше, следуя протоколу исследования.
Во-вторых, в клиническом испытании лечение при помощи «Мезенкьюэ» сравнивалось со стандартной терапией ковида, которая в Израиле осуществляется с применением самых, пожалуй, передовых подходов, чем в среднем по миру. Другими словами, в глобальном масштабе от «Мезенкьюэ» следует ожидать еще более значительного снижения летальности и уменьшения сроков госпитализации.
Для пущего подчеркивания впечатляющей эффективности «Мезенкьюэ» уместно сравнить ее с результативностью противоспалительного препарата «Актемра»/«РоАктемра» (Actemra/RoActemra, тоцилизумаб), блокатором интерлейкина 6 (IL-6) разработки «Рош» (Roche), который, применяясь вместе с глюкокортикостероидами, лишь незначительно, согласно метаанализу, снижает летальность госпитализированных с ковидом пациентов: с 25,8% до 21,8%.

«МИР 19»: новый препарат для лечения коронавируса
Российское лекарство от ковида взяло на вооружение мощную технологию РНК-интерференции.
Что примечательно, 77% пациентов, получавших «Мезенкьюэ», находились в группе повышенного риска плохого прогноза и/или смерти от ковида, так как характеризовались наличием какого-либо из факторов риска (гипертония, гиперлипидемия, ожирение, сахарный диабет 2-го типа). Опять же, лечение «Мезенкьюэ» проводилось в период четвертой волны COVID-19 в Израиле, в которой доминировал дельта-штамм SARS-CoV-2, которому свойственна повышенная летальность.
Поскольку «Мезенкьюэ» действует не против самого коронавируса, но лечит его негативные последствия, терапию не обязательно начинать как можно раньше после манифестации симптомов ковида. Это в корне отличается от подходов, к которым обращаются все противовирусные препараты, в том числе моноклональные антитела, ремдесивир (remdesivir), молнупиравир (molnupiravir), нирматрелвир (nirmatrelvir), фавипиравир (favipiravir), эффективность которых напрямую зависит от сроков давности развития симптоматического COVID-19.
«Бонус Байогруп» уверена, что появление новых штаммов SARS-CoV-2, включая агрессивно распространяющийся омикрон (B.1.1.529), никак не повлияет на заявленную эффективность «Мезенкьюэ». И это очевидно, ведь «Мезенкьюэ», в отличие от противовирусных препаратов, направлен не на борьбу с непосредственно коронавирусом, но острым воспалением и пневмонией, спровоцированными цитокиновым штормом.
«Бонус Байогруп», которая продолжает анализировать собранные в клиническом исследовании фазы II данные, намеревается зарегистрировать «Мезенкьюэ» в Израиле, США и Европе. Регуляторы, скорее всего, истребуют проведения крупномасштабных клинических испытаний фазы III. Впрочем, ввиду неослабевающей ковидной пандемии регуляторные требования, не исключено, будут смягчены.
Расширение производства и доступности «Мезенкьюэ» проблемой не является, поскольку из одного донорского липоаспирата после экспансии и модификации MSC можно получить минимум 45 тыс. доз препарата.