ЧТО ПРОИЗОШЛО
Фрексалимаб (frexalimab) — новый лекарственный препарат, предназначенный для лечения рецидивирующих форм рассеянного склероза.
ОСНОВНЫЕ ФАКТЫ
Фрексалимаб, разрабатываемый «Санофи» (Sanofi), обращается к совершенно иному механизму действия, чем все нынешние препараты, изменяющие течение рассеянного склероза (ПИТРС).
Фрексалимаб, таргетированный на сигнальную ось CD40–CD40L, устраняет как острое, так и хроническое нейровоспаление при рассеянном склерозе, и при этом не вызывает истощения пула B-лимфоцитов, несущее за собой риск тяжелых инфекций и иногда наблюдаемое при применении современных мощных ПИТРС, нацеленных на CD20, таких как «Окревус» (Ocrevus, окрелизумаб), «Кесимпта» / «Бонспри» (Kesimpta / Bonspri, офатумумаб) и «Бриумви» (Briumvi, ублитуксимаб).
Успешно пройдена среднестадийная клиническая проверка, продолжаются длительные регистрационные клинические испытания фазы III.
При благоприятном раскладе «Санофи» в 2027 году отправит в адрес регуляторов досье на регистрацию фрексалимаба.
ПРЯМАЯ РЕЧЬ
«По мере развития науки и диагностических инструментов менялось и наше понимание рассеянного склероза. Теперь мы точно знаем, что ингибирование CD40L приводит к сдерживанию процесса повреждения нервных клеток у людей с рассеянным склерозом. Наша вера в высокоэффективный потенциал фрексалимаба всё больше укрепляется: препарат поможет замедлить или даже остановить прогрессирование этого заболевания».
Патрик Вермерш (Patrick Vermersch), главный автор исследования, вице-президент по исследованиям в области биологии и здоровья в Университете Лилля (Université de Lille, Лилль, Франция).
«Фрексалимаб обладает уникальным механизмом действия, блокируя костимуляционный путь CD40/CD40L, который регулирует активацию и функционирование как адаптивных, так и врожденных иммунных клеток — путь, играющий ключевую роль в патогенезе рассеянного склероза. Та эффективность и скорость, с которой фрексалимаб взял заболевание под контроль, причем без истощения пула лимфоцитов, поразительна».
Гэвин Джованнони (Gavin Giovannoni), заведующий кафедры неврологии в Институте Близарда (Blizard Institute) при Школе медицины и стоматологии Бартса и Лондона (Barts and The London School of Medicine and Dentistry, Barts) в составе Лондонского университета королевы Марии (Queen Mary University of London, QMUL, Лондон, Великобритания).
«Люди с рассеянным склерозом нуждаются в новых высокоэффективных методах лечения, направленных на борьбу с прогрессированием инвалидизации — проблемой, которая по-прежнему остается одним из самых больших незакрытых медицинских вопросов. Результаты клинической проверки фрексалимаба убедительно доказали, что препарат, располагающий новым механизмом действия, способен обеспечить значимые улучшения для пациентов, страдающих этим хроническим и изнурительным заболеванием».
Эрик Вальстрём (Erik Wallström), руководитель глобального подразделения развития неврологии «Санофи» (Sanofi).
СУТЬ ВОПРОСА
CD40 и CD40L (CD154) — костимулирующий белок на поверхности антигенпрезентирующих клеток и его лиганд — играют центральную роль в регуляции гуморального и клеточно-опосредованного иммунитета: взаимодействие CD40 с CD40L на иммунных клетках участвует в активации костимулирующего сигнального пути, контролирующего «перекрестное взаимодействие» между адаптивной и врожденной иммунными системами [1].
Блокада CD40L оказалась эффективной в задаче улучшения экспериментальных аутоиммунных состояний на животных моделях, и поэтому рассматривается привлекательной терапевтической мишенью [2] [3] [4] [5] [6].
Так, на нескольких животных моделях с пептид-индуцированным аутоиммунным энцефаломиелитом (EAE) продемонстрирована функциональная роль сигнального пути CD40–CD40L: короткое профилактическое лечение антителом против CD40L (αCD40L) привело к остановке болезни [5] [7] [8] [9]. Как выяснилось, в центральной нервной системе (ЦНС) взаимодействие CD40–CD40L является критической детерминантой развития и прогрессирования заболевания [10]. Отсутствие экспрессии CD40 клетками, резидентными для ЦНС, уменьшает интенсивность и продолжительность EAE, индуцированного миелиновым олигодендроцитарным гликопротеином, и снижает степень инфильтрации воспалительных клеток в ЦНС. Энцефалитогенные Т-клетки, попадающие в ЦНС, в паренхиматозной микроглии которой CD40 отсутствует, не могут вызвать экспрессию хемокинов в ЦНС.
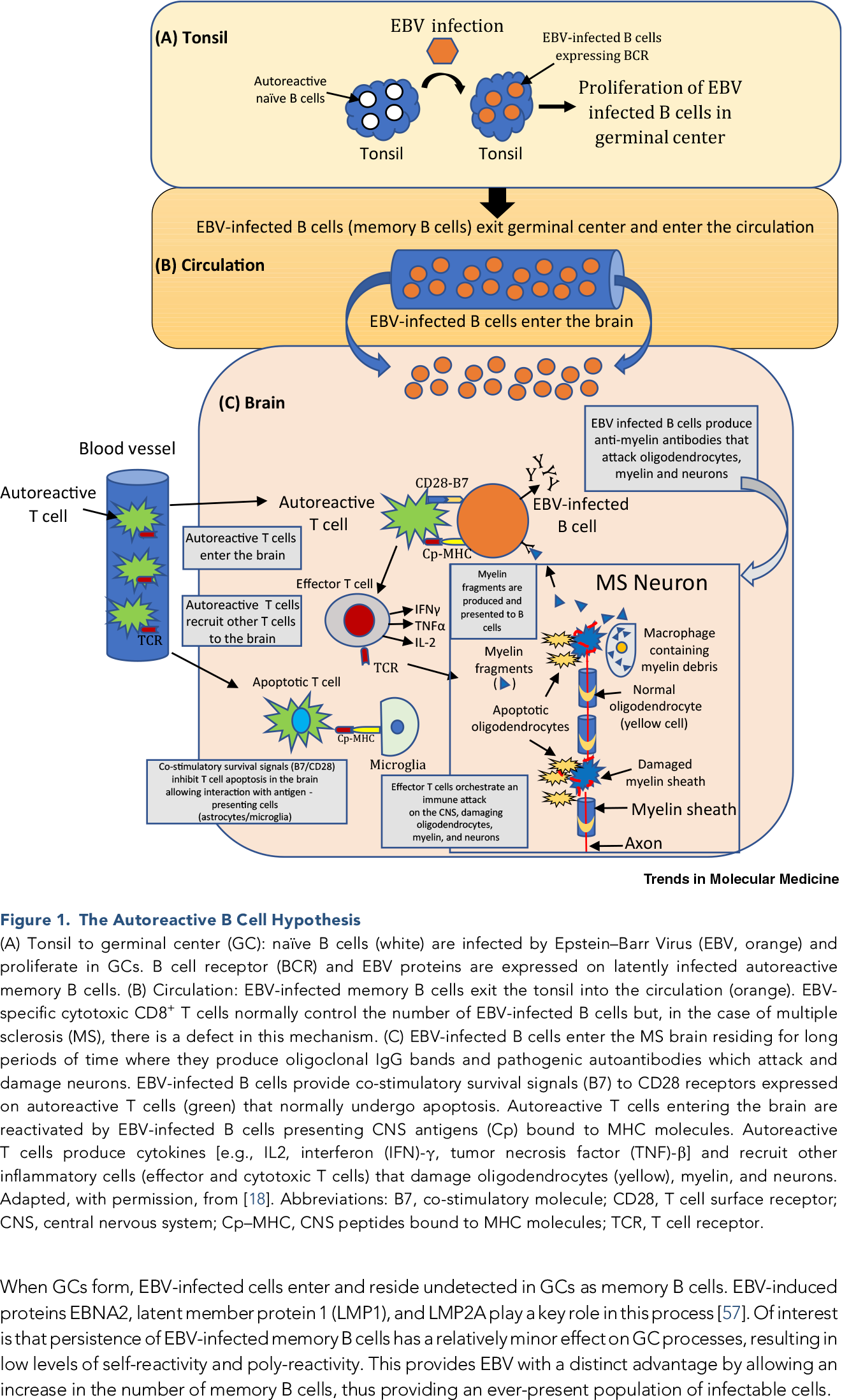
Клинические и патологические наблюдения за людьми c рассеянным склерозом указали на участие сигнального пути CD40–CD40L в развитии и прогрессировании заболевания [11] [12] [13] [14] [15] [16], причем с возможной связью с периферической иммунной толерантностью [17] и инфекцией вирусом Эпштейна — Барр, которая, как было уточнено, индуцирует экспрессию CD40L [18].
При рассеянном склерозе отмечается повышенный уровень экспрессии CD40L на активированных Т-клетках, что приводит к высокому уровню растворимого CD40L, и это в целом коррелирует с клиническим статусом, оцениваемым по расширенной шкале степени инвалидизации (EDSS) [12] [14] [16].
Повышенные концентрации интерферона гамма (IFNγ), обнаруженные у пациентов с рассеянным склерозом, связаны, возможно, с индуцированной CD40L усиленной выработкой интерлейкина 12 (IL-12) или, вероятно, интерлейкина 23 (IL-23) [19] [20] [21].
Выявлены генетические связи между однонуклеотидными полиморфизмами CD40 и риском развития рассеянного склероза [22] [23] [24].
Инфильтрирующие Т-клетки CD40L+ выступают в качестве движущей силы CD40-опосредованного воспалительного ответа и активируют CD40+ моноциты, макрофаги, В-клетки, эндотелиальные клетки и иммунные клетки, обитающие в ЦНС, усиливая поражение рассеянным склерозом и прогрессирование заболевания [25] [26].
Собранные данные подтверждают концепцию, что терапевтическое блокирование взаимодействия CD40–CD40L может быть эффективным подходом к лечению рассеянного склероза.
КАК ЭТО РАБОТАЕТ
Гуманизированное моноклональное IgG1-антитело фрексалимаб (frexalimab, SAR441344, INX-021) связывает CD40L, который экспрессирует на различных клетках, включая активированные T-клетки. Это приводит к ингибированию связывания CD40L с CD40, экспрессирующим на поверхности антигенпрезентирующих клеток (APC). Итогом нарушения сигнального пути CD40–CD40L становится предотвращение T-клеточно-опосредованного иммунного ответа.
Если активированные T-клетки распознают пептид, презентированный B-клетками, CD40L на T-клетках связывается с CD40 на B-клетках, приводя к активации последних. Это влечет за собой деление B-клеток, переключение изотипа антител, дифференцировку в плазматические клетки, вырабатывающие антитела против антигена-мишени. Фрексалимабу по силам сдержать этот каскад.
Выбор лиганда (CD40L), а не рецептора (CD40) в качестве мишени обусловлен рядом моментов. Во-первых, блокируется как непосредственно сигнальная ось CD40–CD40L, так и CD11, костимулирующий рецептор на APC, что приводит к сдерживанию провоспалительной поляризации цитотоксических T-клеток CD8+. Во-вторых, поляризация лимфоцитов CD4+ смещается от провоспалительной сигнализации к анергии и апоптозу T-клеток и насыщенной среде регуляторных T-клеток FoxP3+, тем самым формируя более толерогенную среду. В-третьих, CD40L экспрессирует более избирательно, чем CD40, что усиливает потенциальную безопасность и способствует фармакокинетическим, фармакодинамическим и дозировочным преимуществам.
Важно отметить, что нацеливание на сигнальную ось CD40–CD40L не приводит к истощению пула B-лимфоцитов, то есть нет рисков лимфопении — значит, нивелируются риски ослабления иммунной системы, обычно приводящего к инфекционным заболеваниям.
КЛИНИЧЕСКИЕ ПОДРОБНОСТИ
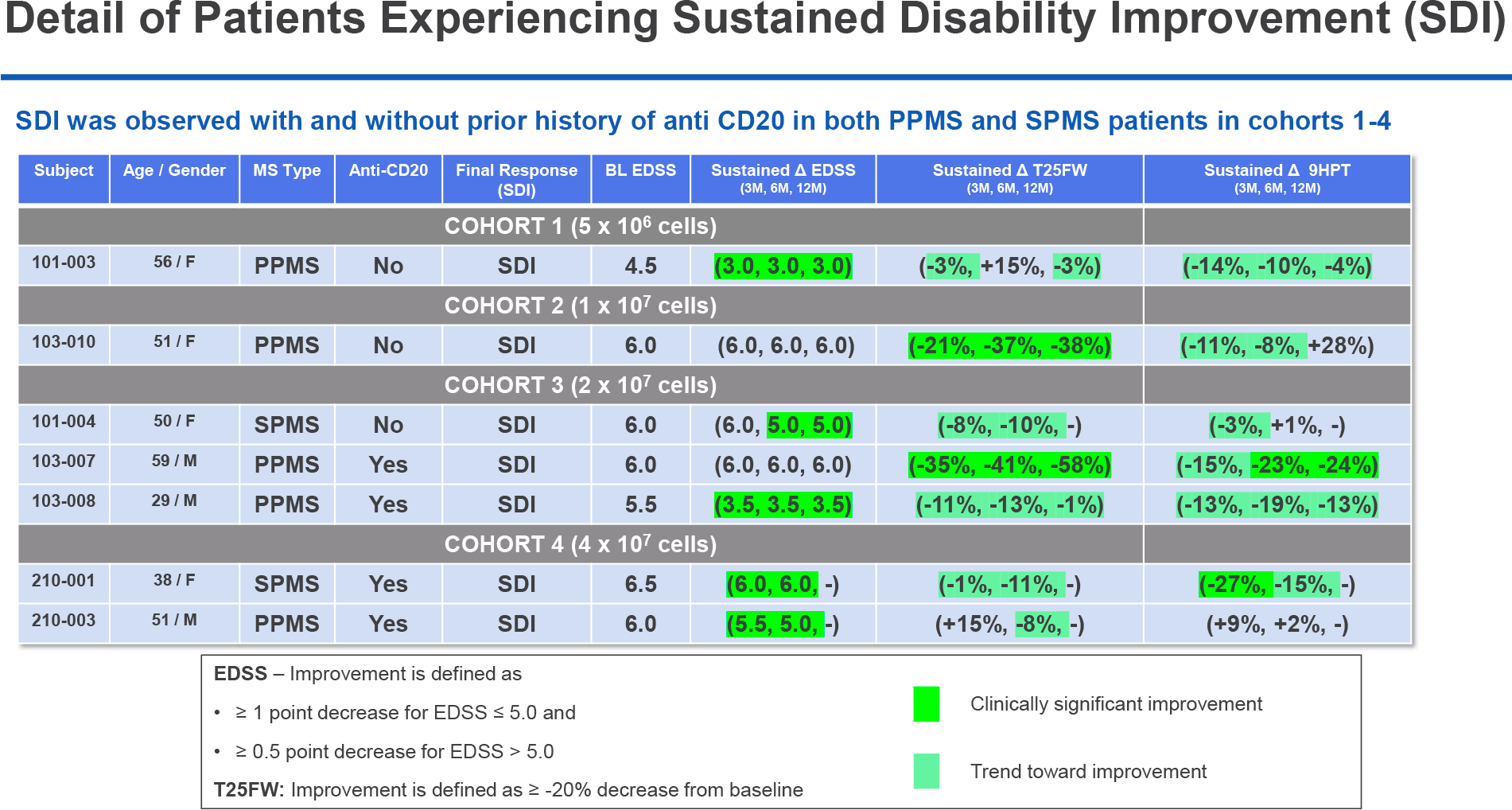
Клиническое исследование NCT04879628 фазы II (рандомизированное, двойное слепое, плацебо-контролируемое, многоцентровое, международное) пригласило взрослых (18–55 лет) пациентов (n=129) с рецидивирующими формами рассеянного склероза (RMS) —рецидивирующе-ремиттирующим рассеянным склерозом (RRMS) или вторично-прогрессирующим рассеянным склерозом (SPMS) с рецидивами.
Среди основных требований к испытуемым: либо как минимум один рецидив в течение предыдущего года, либо два и более рецидива в период двух последних лет, либо не менее одного активного очага поражения головного мозга (на МРТ-изображениях с контрастированием гадолинием) в период последних 6 месяцев до скрининга.
Среди основных характеристик участников: средний возраст 37 лет, 66% женщин, RRMS у 94%, продолжительность заболевания в среднем 7,7 года, балл по расширенной шкале степени инвалидизации (EDSS) медианных 2,5 пункта (2,0–3,5).
Пациентам назначали инъекции либо фрексалимаба в высокой дозе (1200 мг внутривенно каждые 4 недели, плюс 1800-мг нагрузочная доза в первый день) или низкой дозе (300 мг подкожно каждые 2 недели, плюс 600-мг нагрузочная доза в первый день), либо плацебо (по такой же схеме).
По прошествии 12 недель лечения число новых гиперинтенсивных очагов поражения головного мозга на T1-взвешенных МРТ-изображениях с контрастированием гадолинием, как мера активного нейровоспаления, относительно их числа на 8-й неделе составило в среднем 0,2 (95% ДИ [здесь и далее]: 0,1–0,4) и 0,3 (0,1–0,6) в группах высокой и низкой дозы фрексалимаба — против 1,4 (0,6–3,0) в объединенной группе плацебо [1] [2].
Таким образом, применение фрексалимаба снизило вероятность появления новых вышеуказанных очагов на 89% (62–97; p=0,0004) и 79% (44–92; p=0,0021) относительно плацебо: скорректированный относительный риск (risk ratio, RR) 0,11 (0,03–0,38) и 0,21 (0,08–0,56).
При этом 85% и 84% пациентов вообще не отметились появлением новых вышеобозначенных очагов — против 50% в контрольной группе.
Назначение фрексалимаба привело к снижению вероятности появления новых или разрастающихся очагов поражения головного мозга на T2-взвешенных МРТ-изображениях, как мера бремени заболевания, на 92% (74–97) и 86% (59–95): скорректированный RR 0,08 (0,03–0,26) и 0,14 (0,05–0,41). Если в группах фрексалимаба таковых было зарегистрировано 0,3 (0,1–0,6) и 0,5 (0,2–1,0), то в группе плацебо — 3,5 (1,6–7,9).
Схожая картина по сдерживанию T1- и T2-очагов сохранялась и по прошествии 24 недель лечения.
В группах фрексалимаба отмечено снижение уровня циркулирующих биомаркеров нейроаксонального повреждения и воспалительной активности — легкого полипептида нейрофиламента (NfL) и CXC-хемокина 13 (CXCL13). Плазматический уровень первого снизился на 24% и 18%, второго — на 21% и 30%, тогда как в группе плацебо, напротив, отметился подъем этих биомаркеров.
Фрексалимаб характеризовался приемлемой переносимостью. Среди наиболее распространенных нежелательных явлений (НЯ), редких и с легко-умеренной степенью тяжести: коронавирусная инфекция COVID-19 и головная боль. Тромбоэмболических событий не зафиксировано.





По завершении заслепленного периода NCT04879628 испытуемым было предложено перейти к открытому этапу исследования, когда все пациенты получают фрексалимаб, — и 97% участников (n=125/129) на это согласились.
По прошествии 36 недель (всего 48 недель с начала исследования) результаты, собранные среди оставшихся 87% людей (n=112/129), получились следующими [3] [4]:
- 96% и 87% пациентов, которым продолжили назначать соответственно высокую и низкую дозу фрексалимаба, были избавлены от появления новых T1-взвешенных очагов с контрастированием гадолинием.
- Число таких очагов поражения оставалось низким: в среднем 0,0 и 0,2.
- Число и изменение объема новых или разрастающихся T2-взвешенных очагов оставалось низким во всех группах лечения фрексалимабом.
- Количество лимфоцитов было стабильным, уровни иммуноглобулина G (IgG) и иммуноглобулина M (IgM) также были стабильными или чуть снизились.
- В группе высокой дозы фрексалимаба частота рецидивов в пересчете на год (ARR) были низкой, составив 0,04 (0,01–0,18), и 96% пациентов были вообще избавлены от рецидивов, чего не скажешь о группе низкой дозы, в которой ARR вышла к 0,22. Изначально, в предшествовавшем лечению году, число рецидивов было на уровне 1,3±0,6 и 1,2±0,5.
- С начала исследования плазматический уровень NfL продолжал снижаться, и по окончании 48 недель его падение составило 41% и 35%.
- Применение фрексалимаба характеризовалось приемлемой переносимостью. Среди наиболее распространенных НЯ: назофарингит, головная боль, ковид.









После того как прошли 72 недели (18 месяцев или 1,5 года) с начала исследования, в котором оставались 86% испытуемых (n=111/129), результаты получились следующими:
- Совокупное число T1-взвешенных очагов с контрастированием гадолинием: 0,1 и 0,4 — соответственно в группах высокой и низкой дозы фрексалимаба.
- Число новых или разрастающихся T2-взвешенных очагов: 0,1 и 0,4.
- ARR: 0,07 (0,03–0,20) и 0,24, притом что 94% пациентов в группе высокой дозы фрексалимаба не столкнулись с рецидивом.
- Усредненный балл EDSS оставался низким и стабильным.
- Количество лимфоцитов и уровни иммуноглобулина почти не менялись.
- Профиль безопасности фрексалимаба опасений не вызывал.









ЧТО ДАЛЬШЕ
«Санофи» продолжает клиническую проверку фрексалимаба в ходе опорных клинических исследований FREXALT (NCT06141473) и FREVIVA (NCT06141486) фазы III среди пациентов (n=1400 и n=858) соответственно с RMS и SPMS без рецидивов. Первое 3-летнее испытание, которое завершится к середине 2027 года, сравнивает фрексалимаб с «Абаджио» (Aubagio, терифлуномид), второе 4-летнее исследование, результаты которого будут готовы к концу 2026 года, — с плацебо.
ЧТО ЕЩЕ
Фрексалимаб параллельно изучается в лечении других аутоиммунных состояний — первичного синдрома Шегрена и активной системной красной волчанки: в соответствующих клинических испытаниях phaethuSA (NCT04572841) и APATURA (NCT05039840) фазы II.
Фрексалимаб проверяется в FABULINUS (NCT06111586) фазы II на предмет его способности к сохранению функции бета-клеток поджелудочной железы (эндогенной секреции инсулина) при недавно диагностированном сахарном диабете 1-го типа.
Клиническое исследование RESULT (NCT06500702) фазы II сравнивает фрексалимаб с SAR442970, нанотелом против фактора некроза опухоли (TNF) и лиганда OX40 (OX40L), и рилзабрутинибом (rilzabrutinib), обратимым ковалентным ингибитором тирозинкиназы Брутона (BTK), — в ходе лечения первичного фокально-сегментарного гломерулосклероза или первичной болезни минимальных изменений (липоидный нефроз, болезнь Нила).
ЭКСПЕРТНЫЕ КОММЕНТАРИИ
Лечение фрексалимабом рецидивирующих форм рассеянного склероза привело к благоприятным эффектам, которые отразились сдерживанием как появления новых очагов поражения головного мозга, так и разрастания существующих, а также снижением плазматических уровней релевантных биомаркеров. Всё это свидетельствует о благотворном влиянии фрексалимаба, которое проявляется торможением процессов нейроаксонального повреждения и активного нейровоспаления [1] [2] [3] [4] [5] [6].
Поисковый анализ биомаркеров подтвердил состоятельность механизма действия фрексалимаба у пациентов с рецидивирующим рассеянным склерозом: препарат оказывает мощное иммуномодулирующее действие как на врожденные, так и на адаптивные иммунные клетки без истощения лимфоцитов.
Во-первых, анализ иммунофенотипов мононуклеарных клеток периферической крови показал, что после 12 недель лечения фрексалимабом уровень плазмобластов значительно снизился, в то время как общий уровень других популяций иммунных клеток остался неизменным. Во-вторых, препарат снизил уровень циркулирующих белков, участвующих в активации и созревании В-клеток и выработке ими антител, а также белков, экспрессируемых клетками врожденного иммунитета, участвующих в дифференцировке Т-клеток и их миграции через гематоэнцефалический барьер. В-третьих, транскриптомный анализ указал на влияние фрексалимаба на хемокиновую сигнализацию, дифференцировку Т-клеток и сигнальные пути В/Т-клеточных рецепторов.
Ввиду непродолжительности и малого пациентского охвата клинического испытания фрексалимаба нельзя что-либо наверняка утверждать об улучшении клинических исходов. Так, после 12 недель терапии с рецидивом рассеянного склероза столкнулись 0% (n=0/52) и 4% (n=2/51) человек в группах высокой и низкой дозы препарата — против 4% (n=1/26) при назначении плацебо. Изменений балла по расширенной шкале степени инвалидизации (EDSS) не было ни в одной из групп. Отмечены положительные изменения по шкале влияния рассеянного склероза (MSIS-29).
Впрочем, результаты полуторагодичного применения фрексалимаба в высокой дозе, хотя и осуществленные среди очень скромной выборки из 50 пациентов, всё же позволяют сделать достаточно уверенное предположение о его высокой эффективности, если исходить из стабилизации балла EDSS и низкой среднегодовой частоте рецидивов (ARR).
Известные риски, связанные с блокированием CD40L, включают тромбоэмболические события (согласно данным о препаратах первого поколения) [7] [8], повышенную восприимчивость к инфекциям (в том числе оппортунистическим) и реакции гиперчувствительности.
В ходе применения фрексалимаба, при разработке которого был учтен опыт других молекул, несущих риск тромбоэмболических событий, таковых зарегистрировано не было.
Согласно небольшому иммунологическому исследованию торализумаба (toralizumab), моноклонального анти-CD40L-антитела первого поколения, среди пациентов с RRMS, истощения основных подмножеств лимфоцитов периферической крови не выявлено. Напротив, наблюдалось увеличение количества регуляторных Т-клеток и сдвиг в сторону противовоспалительного цитокинового ответа, что указывало на потенциальную индукцию механизмов иммунной толерантности [9].
Клиническая проверка фрексалимаба не зафиксировала истощения B-лимфоцитарного пула. В группе фрексалимаба было зарегистрировано больше инфекций по сравнению с группой плацебо, но серьезных не было. Все случаи коронавирусной инфекции COVID-19 были неосложненными, с легко-умеренной степенью тяжести.
Напротив, лечение рассеянного склероза тем же «Окревусом», моноклональным антителом против CD20, вызывающим деплецию лимфоцитов, приводит к росту риска более тяжелого течения ковида, требующего госпитализации [10], а также серьезных инфекций [11].
БИЗНЕС
«Санофи», занимающаяся фрексалимабом, лицензировала его у «Имьюнекст» (ImmuNext) в рамках соглашения, оформленного в начале января 2017 года. Французский фармацевтический гигант обязался выплатить сумму до $500 млн по мере развития лекарственного актива, плюс роялти от реализации готового препарата [1].
Впрочем, в начале мая 2024 года «Имьюнекст» продала «Роялти фарма» (Royalty Pharma), крупнейшему в отрасли бизнес-аккумулятору роялти, свои права на денежные выплаты от продаж фрексалимаба, взамен получив вознаграждение в размере $525 млн [2].
Согласно отраслевым прогнозам, фрексалимаб, если дополнительно подключит к спектру своих терапевтических показаний лечение системной красной волчанки и сахарного диабета 1-го типа, способен выйти на уровень более чем $5 млрд продаж ежегодно, из которых свыше $3 млрд будут поступать со стороны терапии рассеянного склероза.
Для «Санофи» повышенное внимание к направлению рассеянного склероза важно по ряду причин. Во-первых, «Абаджио» (Aubagio, терифлуномид) начнет терять патентную защиту после 2026 года, хотя первые дженерики, согласно договоренностям, стали появляться уже в марте 2023-го.
Так и случилось: если в период с 2020 года по 2022-й продажи «Абаджио» шли более-менее стабильно, вращаясь вокруг ежегодных €2 млрд, то в 2023 году реализация препарата упала вдвое — до €955 млн.
Во-вторых, терапевтическая эффективность терифлуномида (teriflunomide) серьезно уступает современным ПИТРС, таргетированным на CD20. Речь идет о таких лекарствах, как окрелизумаб (ocrelizumab), офатумумаб (ofatumumab) и ублитуксимаб (ublituximab).

«Окревус»: воодушевление не ослабевает. Но есть нюансы
Немецкие врачи проанализировали окрелизумаб. Его безоговорочная эффективность имеет рамки.
В-третьих, безопасность «Лемтрады» (Lemtrada, алемтузумаб) находится под большим вопросом: существуют риски серьезных сердечно-сосудистых событий, в том числе инсульта и расслоения артерий. Вот почему спрос на «Лемтраду» неуклонно падает: если в 2017 году продажи алемтузумаба (alemtuzumab) вышли к €450 млн, то в 2022-м они снизились до €80 млн, а в 2023-м «Санофи» вообще не включила в финансовый отчет сведения о реализации этого препарата.