ЧТО ПРОИЗОШЛО
«Джемперли» (Jemperli, достарлимаб) обеспечил прежде невиданную ремиссию в ходе лечения рака прямой кишки.
ОСНОВНЫЕ ФАКТЫ
Шестимесячная монотерапия достарлимабом (dostarlimab) местнораспространенного рака прямой кишки с высокочастотной микросателлитной нестабильностью (MSI-H) или дефектами в системе репарации ошибочно спаренных оснований ДНК (dMMR) привела к тому, что после ее завершения больше половины пациентов, для которых были собраны клинические данные, вышли к стойкой ремиссии, которая продолжалась два года.
Никому из ответивших на экспериментальное лечение испытуемых не потребовалось последующее стандартное лечение.
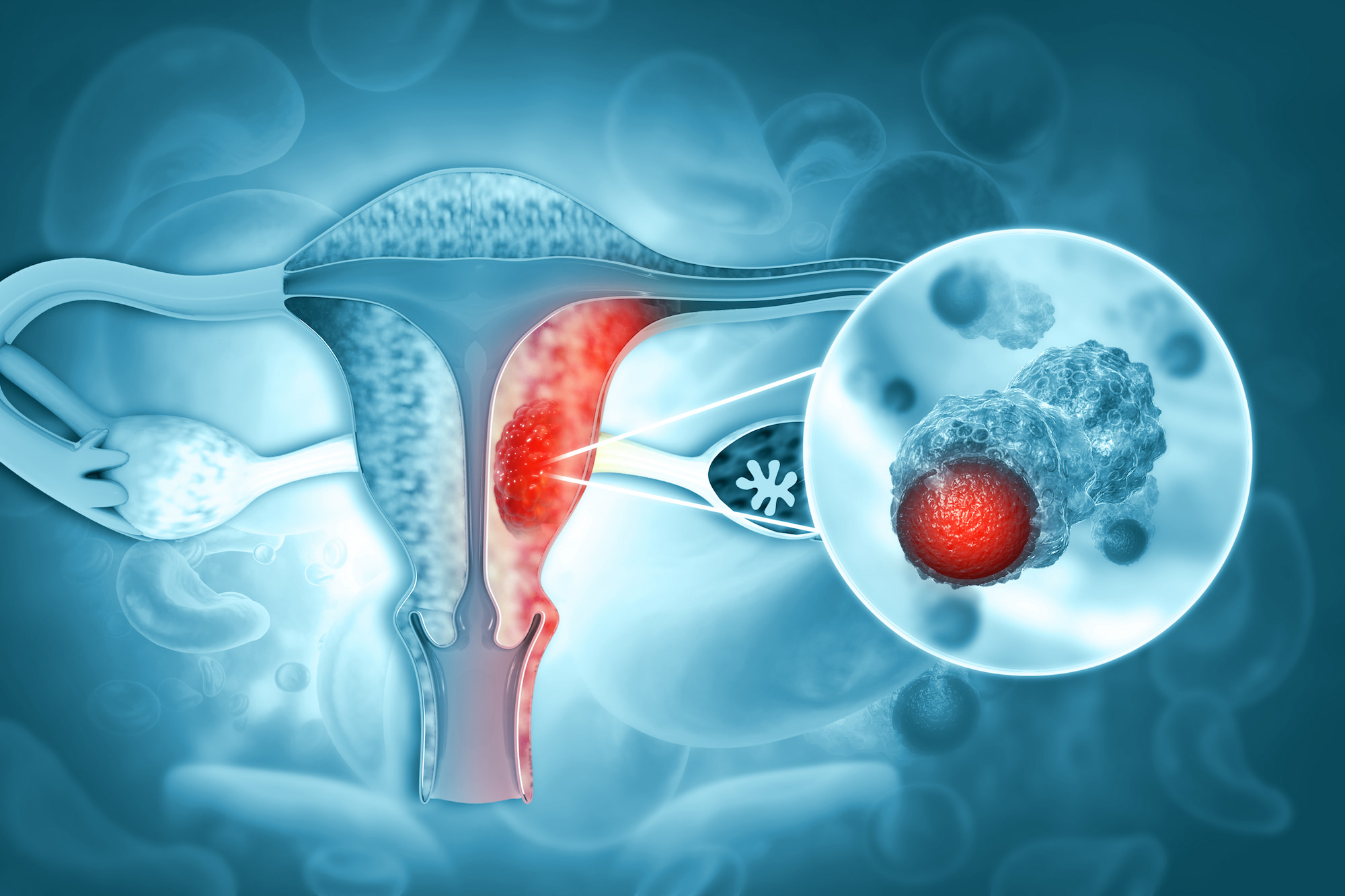
«Джемперли» (Jemperli, достарлимаб), блокатор PD-1, предлагаемый «ГлаксоСмитКляйн» (GlaxoSmithKline), одобрен в лечении рецидивирующих или распространенных солидных опухолей с dMMR/MSI-H, включая рак эндометрия, идущий по отдельному терапевтическому показанию.

«Джемперли»: новый препарат для лечения мутантного рака
Достарлимаб поможет при любых солидных опухолях с MSI-H/dMMR.
«Джемперли» и первоочередное лечение рака эндометрия
Иммунотерапевтический препарат достарлимаб продлит жизнь при распространенном или рецидивирующем раке эндометрия.
ПРЯМАЯ РЕЧЬ
«Достарлимаб, обеспечивший полную ремиссию на протяжении двух лет, должен стать совершенно новым подходом к лечению местнораспространенного рака прямой кишки с MSI-H/dMMR, не требующего стандартного вмешательства с его изнурительными для пациента последствиями».
Андреа Сёрсек (Andrea Cercek), заведующая отделением колоректального рака и содиректор Центра колоректального и желудочно-кишечного рака с ранним началом Мемориального онкологического центра им. Слоуна — Кеттеринга (MSK, Нью-Йорк, США).
«Собранные клинические данные приближают нас к пониманию потенциала достарлимаба в условиях местнораспространенного рака прямой кишки с MSI-H/dMMR. Беспрецедентная 100-процентная частота клинически полных ответов подтверждает грядущее изменение парадигмы лечения этой формы онкологии».
Хешам Абдулла (Hesham Abdullah), старший вице-президент и руководитель глобальных онкологических исследований и разработок «ГлаксоСмитКляйн» (GlaxoSmithKline).
СУТЬ ВОПРОСА
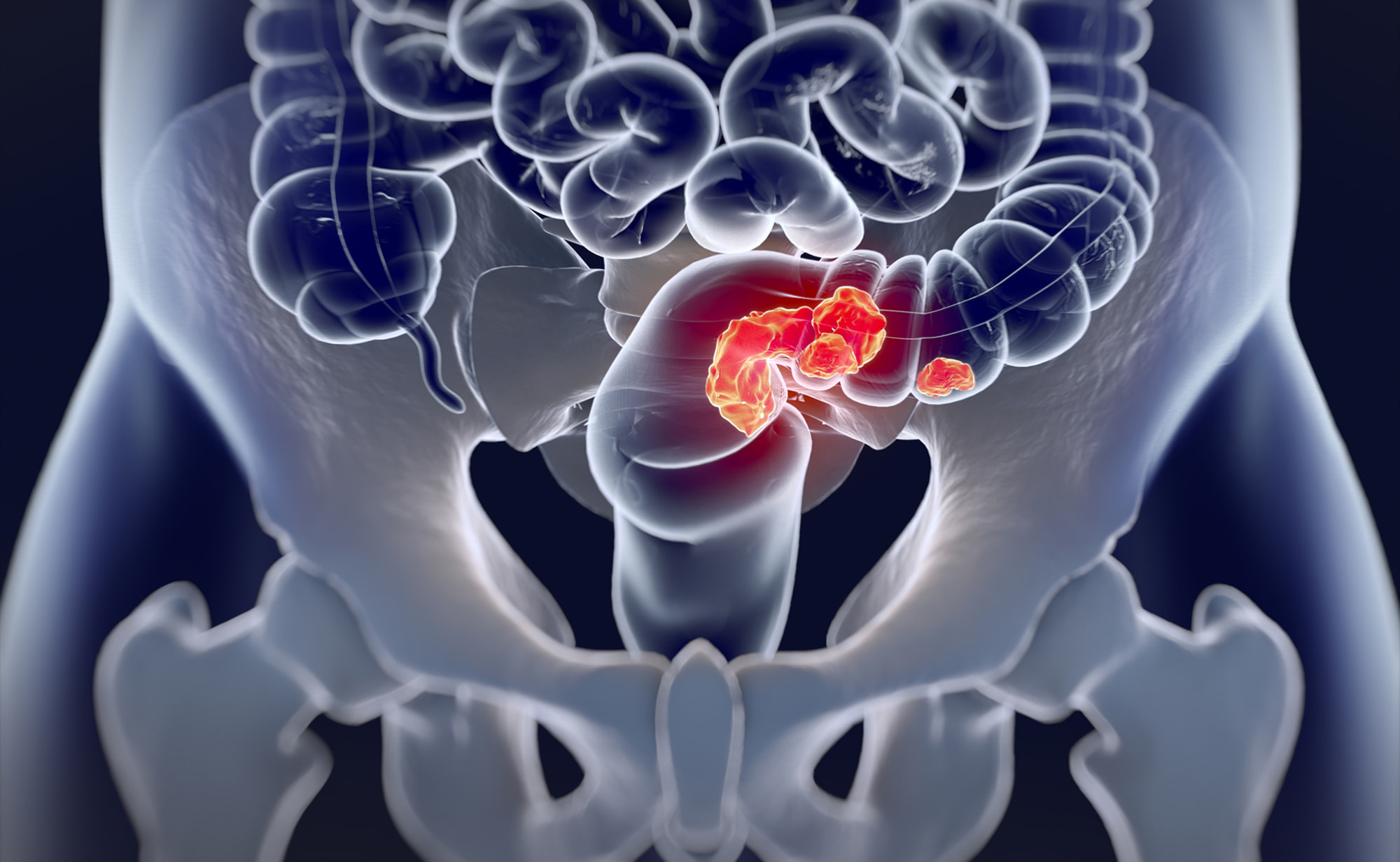
Рак прямой кишки — это форма рака, которая возникает в конечном отделе толстого кишечника и которая обычно относится к группе онкологических заболеваний, называемых колоректальным раком.
Колоректальный рак занимает третье место в мире по частоте диагностирования [1]. Приблизительно в 5–10% случаев рака прямой кишки отмечаются опухолевые аномалии dMMR/MSI-H, влияющие на корректность восстановления ДНК при ее копировании в клетке [2]. Такие аномалии являются биомаркером, который предсказывает успешный ответ на терапевтическую PD-(L)1-блокаду иммунных контрольных точек [3] [4]. Подобные опухоли чаще всего встречаются при раке эндометрия, колоректальном раке и других желудочно-кишечных онкологических заболеваниях, но могут обнаруживаться и при иных солидных опухолях [5] [6] [7] [8].
ПОЧЕМУ ЭТО ВАЖНО
Нынешний стандарт лечения местнораспространенного рака прямой кишки с MSI-H обращается к первоочередному назначению химиотерапии с облучением, затем проводится опухолевая резекция вместе с участками кишечника и/или окружающих тканей [1]. Это приводит к положительным результатам для большинства пациентов, однако почти одна треть больных в конечном итоге умирает ввиду отдаленного метастазирования [2]. Кроме того, оперативное вмешательство и химиорадиотерапия могут отражаться долгосрочными неблагоприятными последствиями, оказывающими серьезное негативное влияние на качество жизни по причине нарушения функции кишечника и мочеиспускания, половой дисфункции, вторичных раковых заболеваний, бесплодия [1].
КЛИНИЧЕСКИЕ ПОДРОБНОСТИ
Клиническое исследование NCT04165772 фазы II (нерандомизированное, открытое, многоцентровое) привлекло взрослых пациентов (n=16) с прежде нелеченной местнораспространенной ректальной аденокарциномой на стадии II/III с MSI-H/dMMR.
Протокол испытания предполагал, что участники получат неоадъювантный (до хирургического вмешательства) достарлимаб (каждые 3 недели на протяжении 6 месяцев), после чего, в случае остаточного заболевания, будет проведена стандартная лучевая терапия с одновременным назначением химиотерапевтического капецитабина, а затем, в случае сохранения заболевания, — тотальное мезоректальное иссечение.
По прошествии медианных 12 месяцев (6–25) наблюдений за пациентами (n=12), которые прошли лечение достарлимабом, результаты получились следующими [1]:
- клинически полный ответ (cCR) составил 100% (95% ДИ [здесь и далее]: 74–100);
- опухоль не обнаруживалась никаким из доступных способов, включая МРТ-изображения, ПЭТ-изображения, эндоскопию, пальцевое ректальное исследование, биопсию;
- прогрессирования или рецидива заболевания не зафиксировано;
- никому из пациентов не потребовались последующие химиорадиотерапия или хирургическое вмешательство.
[su_spoiler class=»my-custom-spoiler» title=»Эволюция эндоскопического и радиографического ответа у пациентов с раком прямой кишки, получавших лечение достарлимабом (dostarlimab). Предупреждение: медицинские изображения могут показаться неприемлемыми.»]


[/su_spoiler]
Столь впечатляющие результаты заставили «ГлаксоСмитКляйн» расширить набор пациентов, чтобы убедиться в высокой эффективности достарлимаба, и она не прогадала.
Так, по прошествии медианных 17,9 месяца (0,3–50,5) наблюдений за испытуемыми (n=42), которые полностью прошли 6-месячный курс лечения при помощи «Джемперли», cCR был зарегистрирован для всех 100% человек [2] [3].
Кроме того, по истечении медианных 26,3 месяца (12,4–50,5) наблюдений, все 24 пациента, для которых был доступен анализ данных, оставались в статусе устойчивого cCR, продолжавшегося как минимум 12 месяцев.
В целом медианное время до фиксирования клинически полного ответа составило 6,22 месяца (6,18–6,45).



ЧТО ДАЛЬШЕ
Продолжается клиническое испытание AZUR-1 (NCT05723562) фазы II, призванное подтвердить успехи достарлимаба в монотерапии прежде нелеченного местнораспространенного рака прямой кишки на стадии II/III (T3–T4, N0 или Tx, N+) с MSI-H/dMMR. Собираются данные, касающиеся пропорции пациентов, сохраняющих статус полной ремиссии по прошествии 12, 24 и 36 месяцев после лечения.
Осуществляется также клиническое исследование AZUR-2 (NCT05855200) фазы III, сравнивающее достарлимаб с химиотерапией в первоочередном лечении колоректального рака на стадии II (T4N0) или стадии III (операбельного) с MSI-H/dMMR. Накапливаются данные по частоте бессобытийной выживаемости (EFS) на протяжении 5 лет после терапии.
ЭКСПЕРТНЫЕ КОММЕНТАРИИ
Победа индукционного неоадъювантного назначения достарлимаба над раком прямой кишки обнадеживает. Облучение и хирургическое вмешательство имеют необратимые последствия для фертильности, сексуального здоровья, функции кишечника и мочевого пузыря [1] [2] [3] [4] [5]. Существенны также последствия для качества жизни, что особенно актуально для молодых людей детородного возраста, поскольку среди них растет заболеваемость раком прямой кишки [6].
Следует, впрочем, понимать, что аденокарцинома прямой кишки только в 5–10% случаев характеризуется наличием MSI-H/dMMR. Такие опухоли весьма плохо отвечают на стандартные схемы химиотерапии, включая неоадъювантную [7] [8] [9].
Важный вопрос заключен в том, почему локализованные опухоли прямой кишки с MSI-H/dMMR реагируют на имммуноонкологическое лечение гораздо сильнее, чем метастатические колоректальные опухоли с MSI-H/dMMR [10].
Одно из объяснений заключается в иммуномодулирующем влиянии микробиома кишечника: некоторые виды бактерий усиливают противоопухолевый иммунный ответ, потенцированный неоадъювантным назначением ингибитора иммунных контрольных точек (ИИКТ) [11] [12] [13]. В ряде клинических испытаний ИИКТ в лечении немелкоклеточного рака легкого (НМРЛ), меланомы и почечно-клеточной карциномы было подтверждено существенное благотворное влияние определенных бактерий кишечного микробиома на противоопухолевый ответ [14] [15] [16].
Кроме того, различия в ответах могут быть связаны с характеристиками опухолевых клеток помимо чрезвычайно высокого мутационного бремени (ввиду нарушенной системы репарации), такими как клональность, анеуплоидия и класс мутации [17] [18] [19].
Если разбивать медианное время до регистрации клинически полного ответа, согласно МРТ прямой кишки, эндоскопии, биопсии, уровню циркулирующей опухолевой ДНК (ctDNA) или ПЭТ-КТ, то оно получилось соответственно равным 6,15 месяца (6,09–6,25), 6,18 месяца (3,62–6,22), 1,41 месяца (1,38–2,73), 1,38 месяца (1,38–2,76) и 2,76 месяца (2,73–6,18).
Получается, что наиболее прогностически ранним оказался высокочувствительный анализ на ctDNA: изначально она обнаруживалась у 97% пациентов, а уже через 6 недель лечения перестала выявляться у более половины участников.
Продолжение наблюдений за пациентами из NCT04165772, чтобы установить окончательную продолжительность ремиссии, позволит выяснить, избавляет ли неоадъюватное иммуноонкологическое лечение от необходимости в хирургической резекции в долгосрочной перспективе.
В будущем, возможно, неоадъюватная блокада PD-1 окажется востребованной в лечении других опухолей с MSI-H/dMMR, таких как локализованный рак поджелудочной железы, желудка, предстательной железы. Следует подтвердить гипотезу востребованности высокоактивной противораковой терапии в неоадъювантном контексте до химиорадиотерапии и хирургического вмешательства, то есть до воздействия других агентов, которые могут нацелиться на клетки с резистентным фенотипом.