БИЗНЕС
Биотехнологический стартап «Митокинин» (Mitokinin), запущенный в 2017 году, занимается разработкой лекарственных препаратов против нейродегенеративных заболеваний, таких как болезнь Паркинсона, болезнь Гентингтона, болезнь Альцгеймера.
Ключевым активом «Митокинин» является MTK458, представляющий собой селективный активатор PINK1 — основного регулятора контроля качества митохондрий, нарушение функций которых, как предполагается, тесно связано с патологическими процессами при нейродегенеративных состояниях.
В начале марта 2021 «ЭббВи» (AbbVie) обзавелась исключительными правами на приобретение «Митокинин». Согласно условиям сделки, компания получила авансовый платеж и продолжила разработку MTK458. Если заявка на проведение клинического испытания нового лекарственного препарата на людях (IND) будет одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), «ЭббВи» возглавит очередь из желающих купить «Митокинин» [1].
Так и произошло. В начале октября 2023 года «ЭббВи» реализовала свое право на приоритетную покупку «Митокинин». Первая заплатила второй 110 млн долларов и еще выплатит до 545 млн долларов по мере реализации лекарственных программ, плюс роялти от продаж готовых препаратов, если таковые будут одобрены [2].
В августе 2020 года «ЭббВи» отказалась от сотрудничества с «Вояджер терапьютикс» (Voyager Therapeutics) в стезе разработки весьма оригинальной генной терапии болезни Альцгеймера, болезни Паркинсона и других нейродегенеративных патологий. Партнеры занимались так называемыми векторизированными антителами, когда нужное моноклональное антитело синтезируется самим организмом — прямиком в головном мозге.

AbbVie отказалась от инновационной генотерапии болезней Альцгеймера и Паркинсона
…когда лекарства синтезируются самим организмом в головном мозге.
ТЕОРИЯ
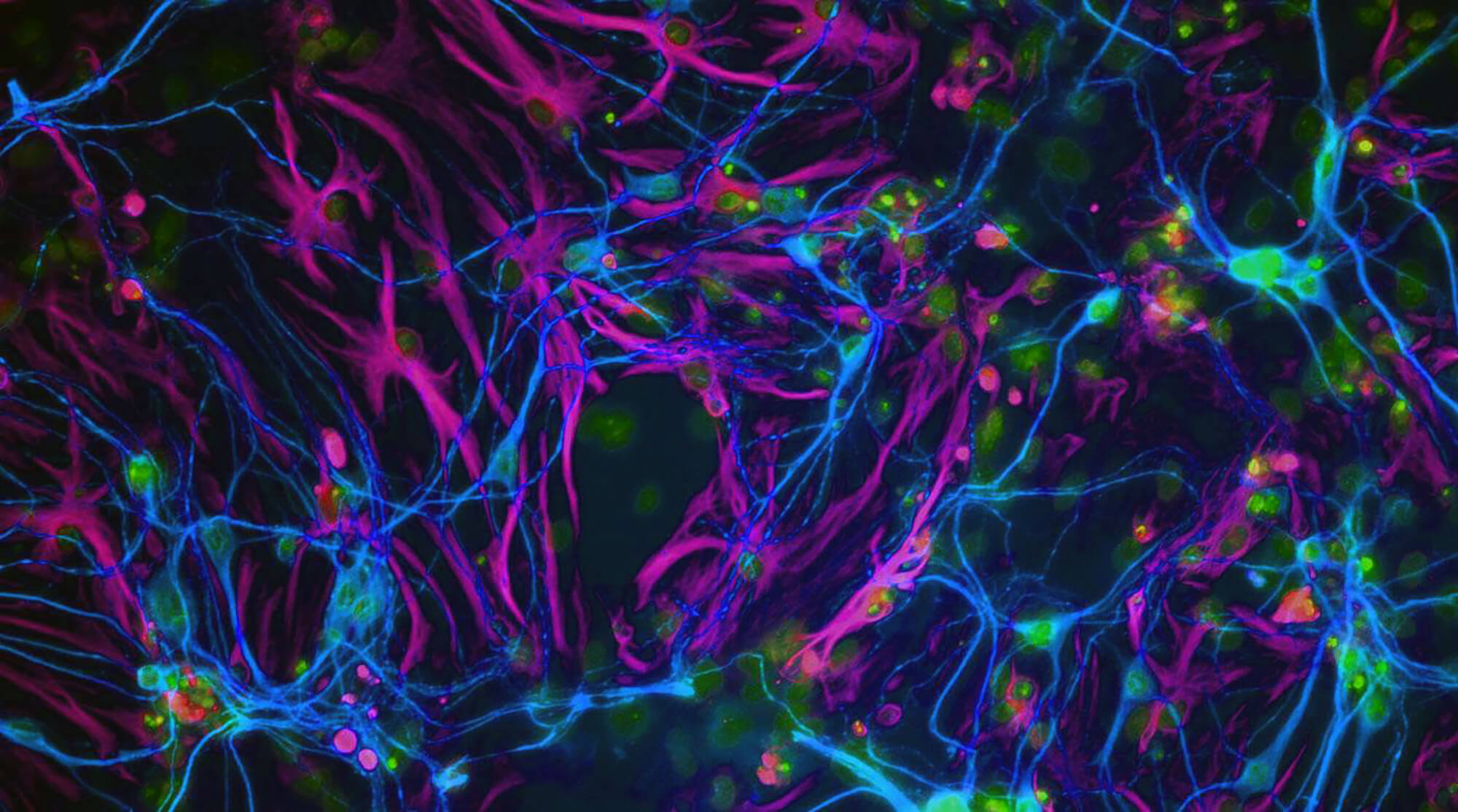
Одной из основных функций митохондрий, органелл большинства эукариотических клеток, является синтез аденозинтрифосфата (АТФ) — универсальной формы химической энергии. Нарушение митохондриальных функций связывают с патогенезом ряда нейродегенеративных заболеваний, поскольку митохондрии задействованы в процессах воспаления, протеостаза и клеточной смерти.
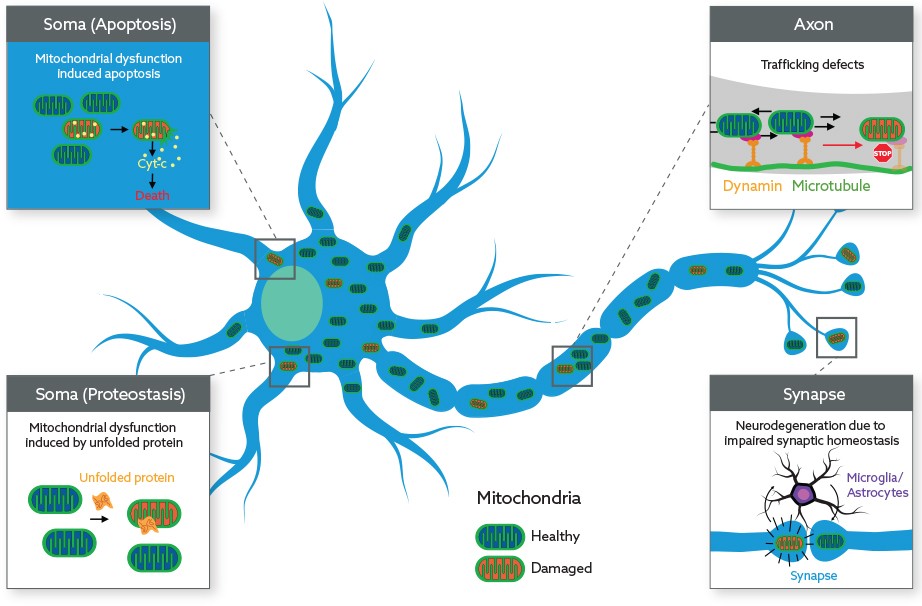
PTEN-индуцированная киназа 1 (PINK1) — главный регулятор контроля качества митохондрий, защищающий клетки от стрессовых дисфункций последних. Если митохондрия каким-либо образом повреждена, PINK1 это выявляет и запускает митофагию — процедуру избирательного разрушения митохондрий путем аутофагии. Активация PINK1 противодействует воспалению, мутациям митохондриальной ДНК (mtDNA), метаболическим и протеостазным сбоям, способным привести к гибели клеток.
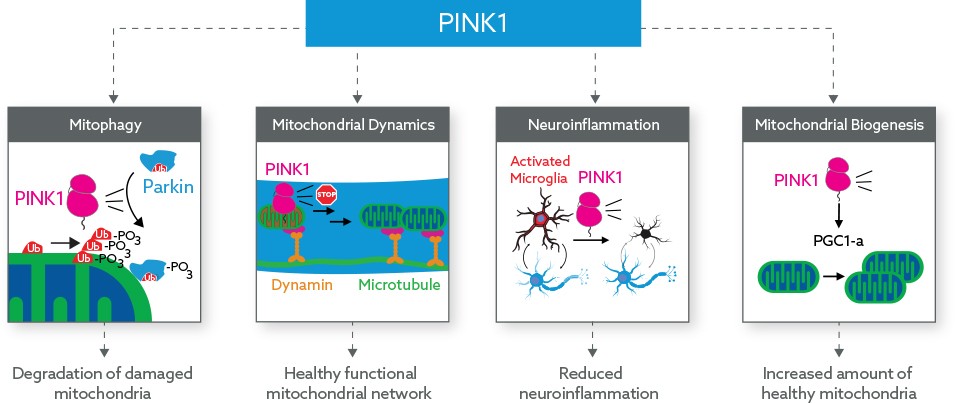
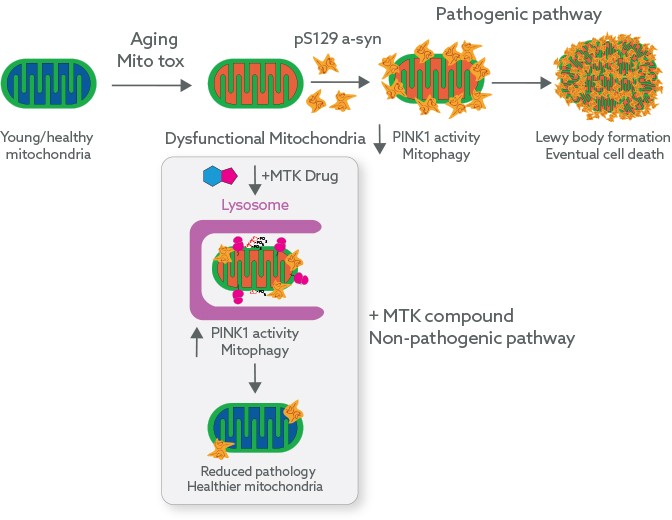
Нейротоксичные белки, вовлеченные в патогенез нейродегенеративных нарушений, такие как альфа-синуклеин, бета-амилоид, тау-белок и TDP-43, ассоциированы с митохондриями и их дисфункцией. Митофагия, посредством которой клетки избавляются от поврежденных митохондрий, играет важную защитную роль в условиях нейродегенеративных состояний, восстанавливая пул нормальных митохондрий и осуществляя клиренс протеотоксинов. Как полагает «Митокинин» (Mitokinin), потенцирование сигнального пути PINK1 при наличии протеотоксического стресса может восстановить здоровое состояние нейронов и сдержать или даже устранить патологические процессы, задействованные при нейродегенеративных заболеваниях [1].
Лекарственные средства, таргетированные на киназы, разрабатываются уже свыше 30 лет. Подавляющее большинство таких препаратов ориентировано на ингибирование киназ, то есть снижение или блокирование их сигнальной активности. Так, например, появившийся в 1995 году в Японии фасудил (fasudil), первый низкомолекулярный антикиназный лекарственный препарат, нацелен на ингибирование Rho-ассоциированной протеинкиназы (ROCK), что востребовано при спазме сосудов головного мозга [2].
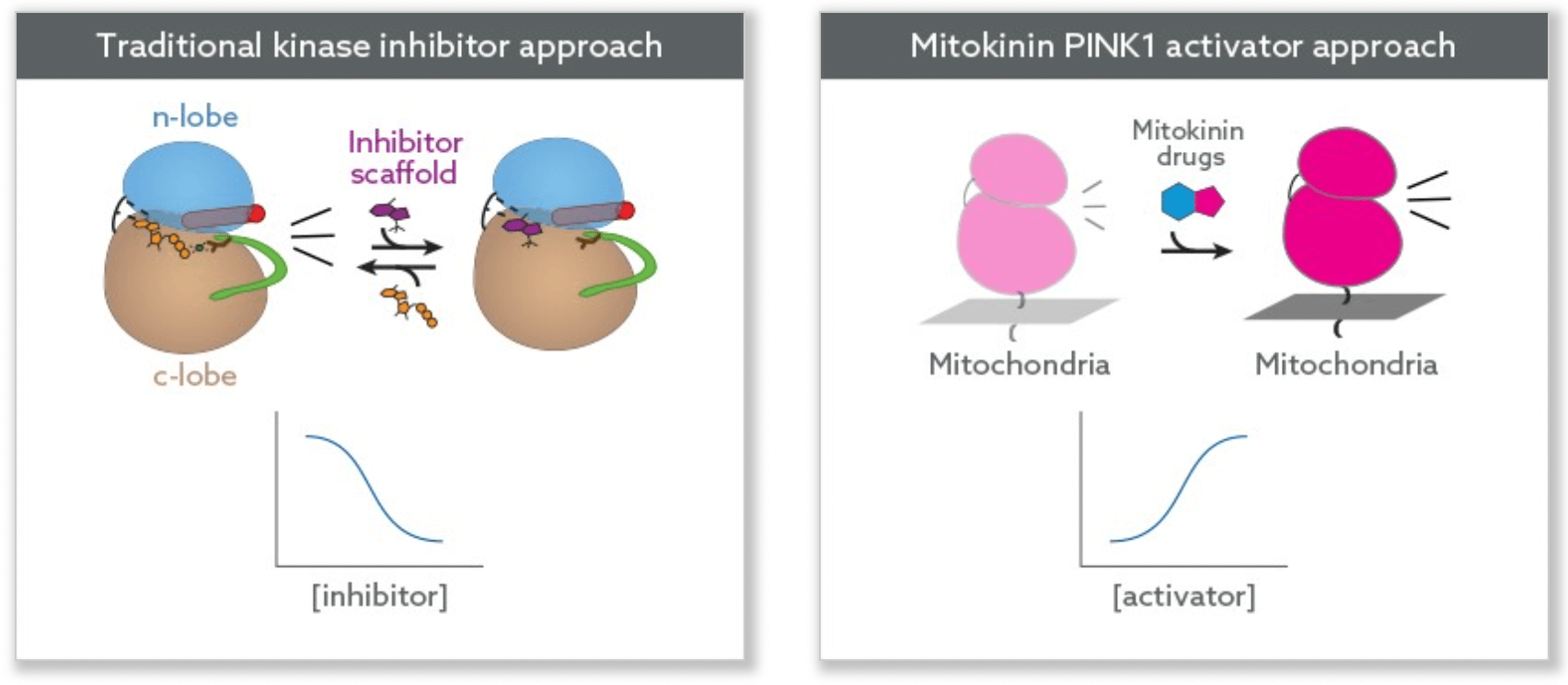
Терапевтический подход, организованный «Митокинин», обращается, напротив, к усилению киназной активности, причем он нацелен исключительно на уже активированную PINK1. Ввиду того, что уровни активной формы PINK1 весьма тщательно регулируются на клеточном уровне, когда эта киназа становится каталитически активной на поверхности только поврежденных митохондрий, разрабатываемые «Митокинин» лекарственные соединения характеризуются высокой избирательностью и не затрагивают процессы активации или деградации PINK1.

Ведущий препарат-кандидат MTK458 прошел тщательную проверку in vitro и in vivo на животных моделях болезни Паркинсона.
Параллельно MTK458 тестируется на моделях болезни Гентингтона, болезни Альцгеймера, а также связанных со старением заболеваний, к которым причастны митохондриальные дисфункции.
Осталось осуществить клинические испытания на людях: экспериментальное лечение должно быть изучено, скорее всего, среди пациентов с аутосомно-рецессивной болезнью Паркинсона с ранним началом.
Факт того, что некоторые типы клеток в центральной нервной системе более склонны к нейродегенерации при болезни Паркинсона, является общепризнанным, однако недостаточно изученным. Ряд уязвимых клеточных субпопуляций, в том числе дофаминовые нейроны в компактной части черного вещества (substantia nigra pars compacta), располагают общим фенотипом крупных и обширных аксональных сетей, плотных синаптических связей и высокого базального уровня нейронной активности. Указанные особенности требуют значительных биоэнергетических затрат, и это позволяет предложить, что данные нейроны испытывают митохондриальный стресс высокой степени напряжения. Вот почему критически важно обратить внимание на механизмы контроля качества митохондрий, поскольку они играют определяющую роль в поддержании выживаемости нейронов [3].
Независимая группа исследователей пришла к выводу, что PINK1 — общая аутоантигенная мишень Т-клеток при болезни Паркинсона, причем преимущественно у лиц мужского пола. Собранные результаты подтвердили целесообразность изучения этого заболевания в контексте иммунной системы: возможно, получится разработать персонализированные иммунологические методы его лечения [4].
«Митокинин» установила, что патологический альфа-синуклеин локализуется в митохондриях, вызывая дисфункцию митохондрий, нарушение митофагии и накопление субстрата PINK1 — pS65-убиквитина (pUb). Отталкиваясь от химии единственного известного активатора PINK1, кинетина (kinetin), исследователи синтезировали сотни его аналогов, в итоге выбрав единственный — MTK458. Эта молекула, способная миновать гематоэнцефалический барьер (ГЭБ), связывается с активной формой PINK1 и стабилизирует ее активный комплекс, тем самым повышая активность, активируя митофагию и ускоряя клиренс аккумулированных pUb и альфа-синуклеина.
В клеточных и животных моделях болезни Паркинсона активация PINK1 с помощью MTK458 ослабила характерную патологическую агрегацию альфа-синуклеина, митохондриальную дисфункцию и остановку митофагии. Отмечено снижение уровня pUb — специфического для PINK1 биомаркера и индикатора митохондриального стресса.

ПРАКТИКА
«ЭббВи» (AbbVie) осуществляет клинические испытания, NCT06414798 и NCT06579300 фазы I, изучая безопасность, переносимость и фармакокинетику ABBV-1088 (MTK458) среди взрослых добровольцев.
ДОПОЛНИТЕЛЬНЫЕ МАТЕРИАЛЫ
Pharmacological PINK1 activation ameliorates pathology in Parkinson’s disease models. Res Sq [Preprint]. 2024 May 10:rs.3.rs-4356493. [источник]
PINK1 is a target of T cell responses in Parkinson’s disease. bioRxiv [Preprint]. 2024 Feb 12:2024.02.09.579465. [источник]
PINK1 and Parkin mitochondrial quality control: a source of regional vulnerability in Parkinson’s disease. Mol Neurodegener. 2020 Mar 13;15(1):20. [источник]
A neo-substrate that amplifies catalytic activity of parkinson’s-disease-related kinase PINK1. Cell. 2013 Aug 15;154(4):737-47. [источник]
PINK1-induced mitophagy promotes neuroprotection in Huntington’s disease. Cell Death Dis. 2015 Jan 22;6(1):e1617. [источник]
PINK1 signalling rescues amyloid pathology and mitochondrial dysfunction in Alzheimer’s disease. Brain. 2017 Dec 1;140(12):3233-3251. [источник]
The PINK1-PARKIN mitochondrial ubiquitylation pathway drives a program of OPTN/NDP52 recruitment and TBK1 activation to promote mitophagy. Mol Cell. 2015 Oct 1;60(1):7-20. [источник]